Un mismo comportamiento farmacocinético, es la PRUEBA para GARANTIZAR el mismo efecto farmacodinámico.
Sección dedicada exclusivamente a reforzar los conceptos detrás de la bioequivalencia de los medicamentos Normon. A continuación verá un video explicativo, y en la parte inferior puede encontrar preguntas y respuestas frecuentes alrededor del tema.
NORMON ES BIOEQUIVALENCIA REAL
Como introducción presentamos un video producido y publicado por Laboratorios Normon. Productos con bioequivalencia, desde su nacimiento.
PREGUNTAS FRECUENTES - BIOEQUIVALENCIA
-
Existen dos tipos de medicamentos: el innovador y el genérico.
El medicamento genérico es creado para ser o tratar de ser igual a un medicamento innovador en cuanto a su dosificación, seguridad, potencia, vía de administración, calidad, características de rendimiento y uso previsto.
Vale recalcar que también existen genéricos puros y genéricos con nombre fantasía; sin embargo un nombre de fantasía no lo desprende de su naturaleza genérica. Esta táctica de nombres fantasia ha sido la que han usado algunas empresas de medicamentos genéricos, que tal vez quieren insinuar que no lo son. Sin embargo, esa posición es utópica: por definición, un medicamento que no es innovador lo hace automáticamente un genérico.
-
Con pruebas de bioequivalencia clínica.
Así es como un medicamento genérico demuestra que funciona de la misma manera y proporciona el mismo beneficio clínico que su versión innovadora. En otras palabras, usted puede sustituir su medicamento innovador con un medicamento genérico bioequivalente sin ninguna duda.
Las pruebas de bioequivalencia son usualmente costosas, de difícil acceso y rondando los cientos de miles de dólares por producto. Puede explicar que quizá no cualquier fabricante puede hacerlas, y/o no para todos sus productos.
Fuente: U.S. FOOD AND DRUG ADMINISTRATION. FDA: Medicamentos Genéricos: Preguntas y Respuestas
Un medicamento que no es original, y no tiene pruebas de equivalencia, se le considera una “copia”.
-
Las consideraciones pueden ser muchas, sin embargo existen algunas básicas que deben de respetarse siempre.
Los estudios se basan en el principio de que en una misma persona, si un mismo principio activo contenido en dos medicamentos similares (la especialidad genérica y la de referencia) se absorbe en la misma cantidad y velocidad en sangre, se hallará en el lugar donde ejerce la acción en una concentración similar ejerciendo entonces un efecto terapéutico también similar.
Aparte de las pruebas clínicas con personas sanas (in vivo), se complementan con otro tipo de pruebas químicas de laboratorio llamadas “pruebas de disolución” (in situ). Sin embargo estas pruebas “in situ” son tan solo complementarias, son menos complejas, y por sí solas no pueden determinar que un medicamento es bioequivalente.
-
Sí.
Cualquier medicamento genérico con pruebas de bioequivalencia efectivas contra un medicamento innovador como modelo debe tener los mismos efectos en el cuerpo que ese medicamento de marca.
Un medicamento genérico bioequivalente es igual que un medicamento innovador en cuanto a su dosificación, seguridad, efectividad, potencia, estabilidad y calidad, así como en la forma en que se toma y la forma en que se debe utilizar.
Los medicamentos genéricos bioequivalentes utilizan los mismos ingredientes activos que los medicamentos de marca y funcionan de la misma manera, por lo que tienen los mismos riesgos y beneficios que los medicamentos de marca.
-
No, los genéricos bioequivalentes producen los mismos efectos y en el mismo periodo de tiempo que el medicamento original de marca. Deben demostrar su bioequivalencia terapéutica en comparación con el medicamento original por medio de estos estudios.
Un medicamento genérico (con o sin marca fantasía) y sin pruebas de bioequivalencia (en otras palabras - una “copia”) sí pueden tener respuestas diferentes al original como tardar más tiempo en surtir efecto. Fuente: Gobierno de España. Preguntas frecuentes de medicamentos genéricos.
-
Si, son intercambiables. Para ser autorizados por la Agencia Española de Medicamentos y Productos Sanitarios, deben demostrar su bioequivalencia terapéutica con el medicamento original de marca que le sirve de referencia, por medio de estudios de biodisponibilidad.
-
Siempre habrá un nivel leve de variabilidad natural que carece de importancia médica, tal como lo hay para un lote de medicamento de marca en comparación con el siguiente lote del mismo producto de marca. Esta variabilidad puede ocurrir y ocurre durante la fabricación, tanto para medicamentos de marca como para medicamentos genéricos. Cuando un medicamento, genérico o de marca, se produce en masa, se permiten variaciones muy pequeñas en la pureza, el tamaño, la potencia y otros parámetros. Las autoridades sanitarias en todo el mundo son las responsables de definir los límites de cuánta variabilidad es aceptable..Existen ejemplos de respuestas variables de medicamentos de marca y de medicamentos genéricos bioequivalentes?
Por ejemplo, en un estudio de investigación muy extenso en el que se compararon medicamentos genéricos con medicamentos de marca, se descubrió que existían diferencias muy pequeñas (de aproximadamente 3.5 %) en la absorción en el cuerpo entre medicamentos genéricos y de marca. Algunos genéricos fueron absorbidos un poco más, algunos ligeramente menos. Esta diferencia es de esperar y aceptable, ya sea para un lote de medicamento de marca evaluado en comparación con otro lote de la misma marca o para un medicamento genérico evaluado en comparación con un medicamento de marca. Como regla general, la diferencia entre la comparación del medicamento genérico al de marca fue la misma que la comparación del medicamento de marca a marca.
Fuente: Davit et al. Comparing generic and innovator drugs: a review of 12 years of bioequivalence data from the United States Food and Drug Administration (“Comparación de medicamentos genéricos e innovadores: una revisión de 12 años de datos de bioequivalencia de la Administración de Alimentos y Medicamentos de los Estados Unidos”). Ann Pharmacother. 2009; 43(10):1583-97.
-
Los medicamentos o fármacos genéricos solo se hacen disponibles después de una examinación rigurosa por parte de la FDA y después de un período de tiempo determinado de exclusividad de la versión de marca en el mercado. Esto se debe a que los medicamentos nuevos, generalmente están protegidos por patentes que prohíben que otros fabriquen y vendan copias del mismo medicamento.
Una patente protege la inversión de la compañía en el desarrollo del medicamento al otorgar a la empresa el derecho exclusivo de vender el medicamento mientras la patente esté vigente.
La FDA también otorga ciertos períodos de exclusividad que pueden prohibir la aprobación de medicamentos genéricos.
Una vez que estas patentes y exclusividades de comercialización caducan, se puede aprobar el medicamento genérico.
Los medicamentos genéricos también tienden a costar menos que sus equivalentes de marca porque los fabricantes de medicamentos genéricos solicitantes no tienen que repetir los estudios en animales y otros estudios clínicos que fueron exigidos para demostrar su seguridad y eficacia.
De hecho, a menudo se aprueban aplicaciones de múltiples empresas para comercializar un solo producto; esto crea competencia en el mercado que generalmente resulta en precios más bajos.
La reducción del costo inicial de investigación significa que, aunque los medicamentos genéricos tienen el mismo efecto terapéutico que sus equivalentes de marca, generalmente se venden con descuentos sustanciales, alrededor de 50%-80% menos en comparación con el precio del medicamento de marca. Según el IMS Health Institute, los medicamentos genéricos ahorraron $1,67 trillones al sistema de salud estadounidense entre 2007 y 2016.
-
Las principales ventajas de los medicamentos genéricos son la experiencia de uso en la práctica clínica y el ahorro.
La experiencia de uso en la práctica clínica porque su principio activo lleva al menos 10 años en el mercado. Su menor precio se traduce en un beneficio directo para el ciudadano al pagar menos por el medicamento, al tiempo que contribuyen a racionalizar el gasto público en medicamentos, pero manteniendo la calidad y la eficacia de la prestación farmacéutica.
-
No.
En Costa Rica la oferta de medicamentos genéricos bioequivalentes es de alguna manera limitada, y la gran mayoría de medicamentos genéricos puros y con nombre fantasía no tienen estas pruebas. Son muy pocos los laboratorios que en el año 2024 sean reconocidos por portafolios de productos 100% bioequivalentes desde su nacimiento. Laboratorios Normon es uno de ellos y ofrece productos bioequivalentes hasta a un mejor precio que algunos genéricos fantasía que no tienen esa garantía.
La gran mayoría de oferentes en el mercado no presentan estas pruebas, por lo que no se consideran bioequivalentes sino que copias.
-
En Costa Rica, el Ministerio de Salud. En el siguiente vínculo podrá encontrar la lista de medicamentos que requieren de pruebas de bioequivalencia para otorgar o renovar su registro sanitario: Ministerio Salud CR - Listado de productos de referencia
Por otro lado, en el caso del origen de Laboratorios Normon, la encargada es la Agencia Española de Medicamentos y Productos Sanitarios del Ministerio de Sanidad, Política Social e Igualdad.
En España, todos los medicamentos de uso humano de fabricación industrial deben contar con los requisitos establecidos de calidad, pruebas completas de bioequivalencia (in vivo e in situ), y pruebas de seguridad y eficacia, para obtener la autorización de comercialización de la Agencia.
La Agencia, en el proceso de autorización de comercialización de un medicamento genérico exige los mismos requisitos que para un medicamento original excepto los estudios preclínicos y clínicos del principio activo (que están ya realizados para el medicamento original de marca).
-
Si. La Ley 29/2006, del 26 de julio, establece los requisitos de calidad exigibles a los principios activos que se utilizan en la fabricación de medicamentos, que son establecidos mediante el Real Decreto 824/2010, de 25 de junio, por el que se regulan los laboratorios farmacéuticos, los fabricantes de principios activos de uso farmacéutico y el comercio exterior de medicamentos y medicamentos en investigación.
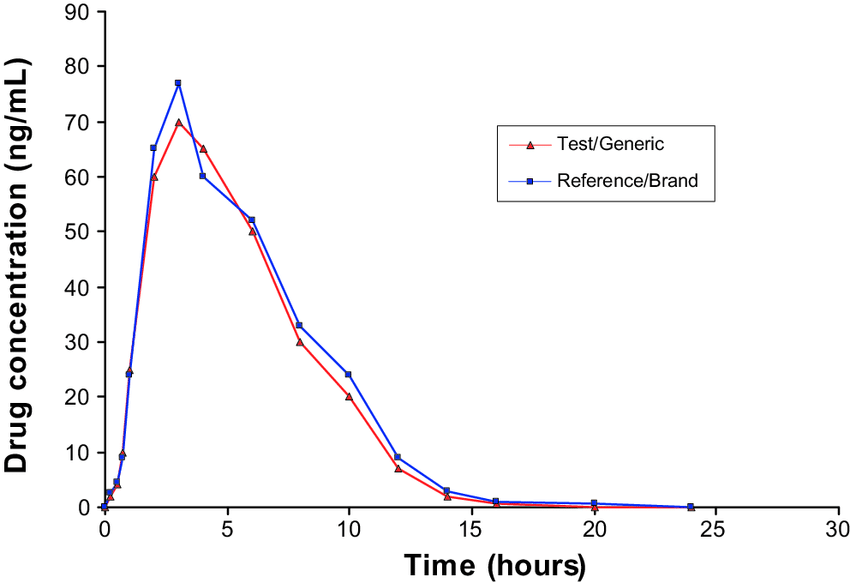
Ejemplo de una gráfica comparativa en un estudio de bioequivalencia. Las líneas de color representan al medicamento original versus un genérico. Una vez ingerido el medicamento y con el paso del tiempo, las concentraciones en sangre inicialmente aumentan, y luego van bajando conforme el medicamento se elimina. Un medicamento bioequivalente debe mostrar curvas similares, e indicadores como Tmax y área bajo la curva al compararse contra el innovador, tal como se muestra en la figura.